AKTUELLES
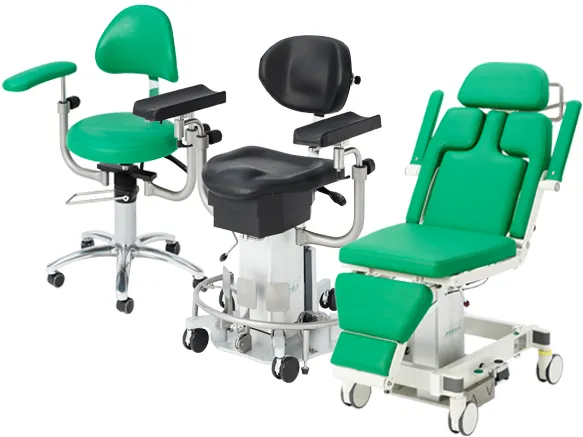
PRODUKT-HIGHLIGHTS

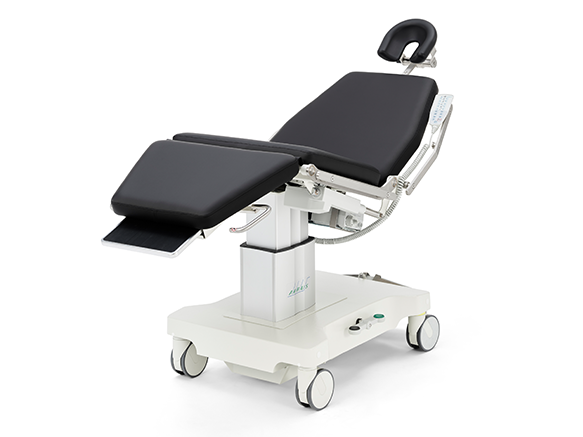
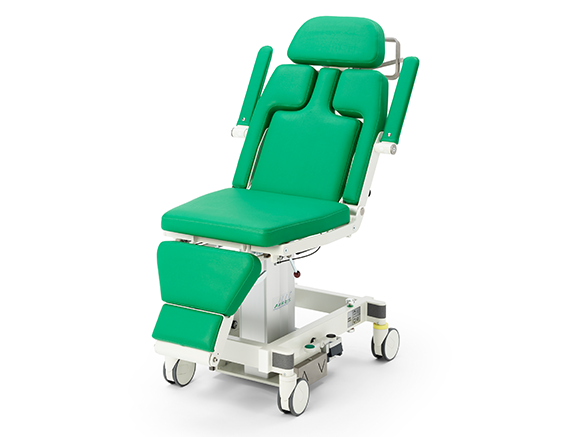
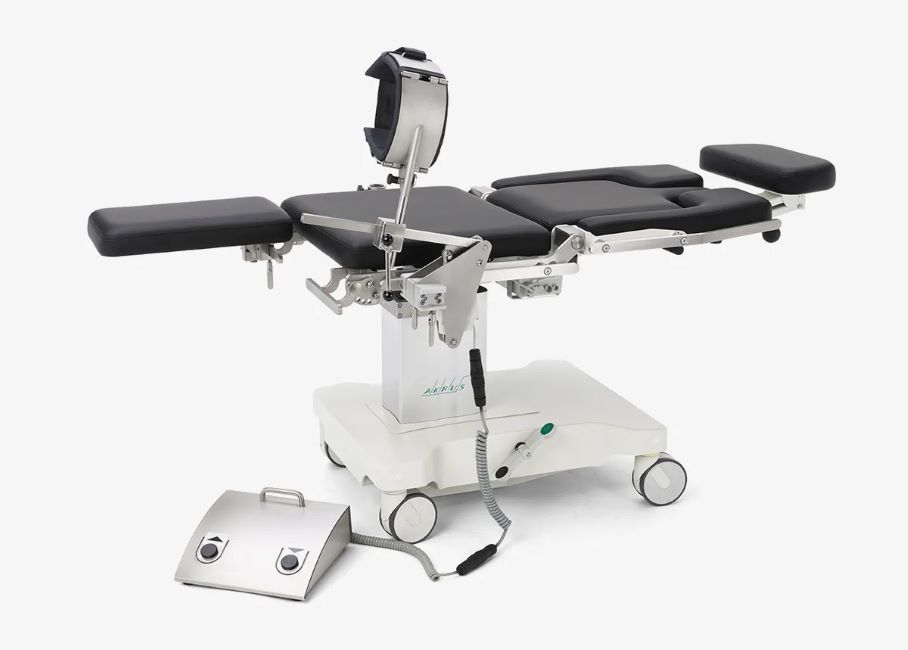
ak5010 MBS
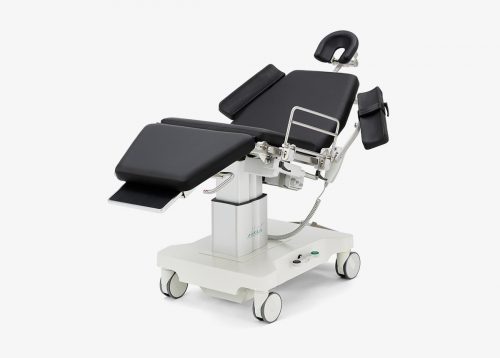
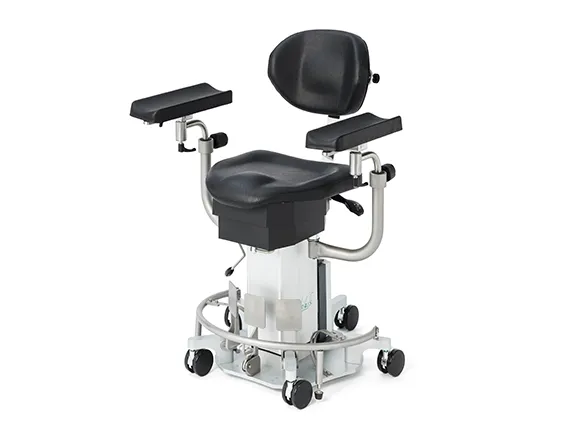
sc5010 ES
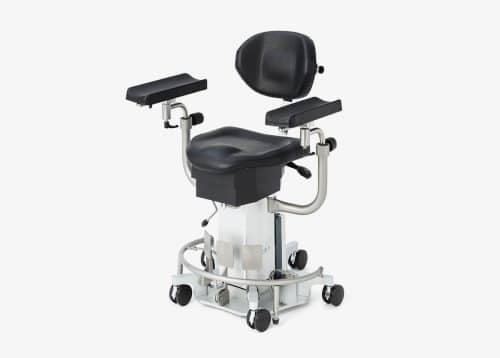
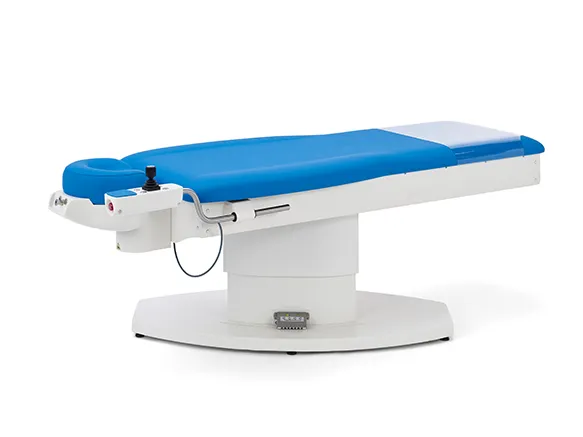
ak480
WIR BIETEN MOBILE LÖSUNGEN
Unsere Mission ist es, Operateure und Industriepartner auf der ganzen Welt mit Patientenlagerungssystemen zu unterstützen, die im Rahmen ambulanter Eingriffe, präzise operative Ergebnisse mit einem ergonomischen Arbeitsablauf ermöglichen.
- Mobile OP-Stühle & Liegen für ambulante Eingriffe
- Flexible und ergonomische Arbeitsabläufe
- Zubehör zur Funktionserweiterung
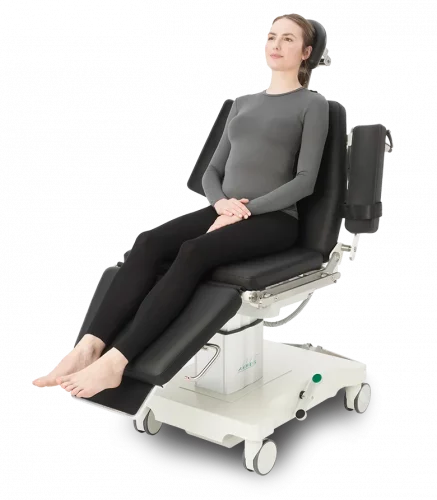
Der ak 5010 MBS ist ein technisch und ergonomisch speziell entwickelter Stuhl für die Lagerung und den Transport von Patientinnen.
Typische Anwendungsgebiete sind HNO, MKG. Plastische, rekonstruktive & ästhetische Chirurgie (Kopfbereich) sowie Nervenstimulation und Blutspenden.
MOBILE.
ERGONOMIC.
RELIABLE.

AKRUS GmbH & Co. KG
ENTDECKEN SIE UNSERE PRODUKTE
Management System Certificate
AKRUS ist zertifiziert nach ISO 13485:2016. Die von uns vertriebenen Produkte sind als Medizinprodukte der Klasse 1 zugelassen. Damit folgen wir den Regularien der europäischen MDR Verordnung (Medical Device Regulation). Wir bieten CE zertifizierte Produkte an. Die Vorteile für unsere Kunden und Anwender sind bspw. die sichergestellte Chargenrückverfolgung, die Ankündigung von Produkt- und Teilelieferungen, ein stabiler und gleich bleibender Herstellungsprozess, sowie eine Risikominimierung durch Prozessorientierung. Für unsere Fachhandelskunden bedeutet unsere Zertifizierung darüberhinaus, dass ihrerseits auf das Lieferantenaudit verzichtet werden kann.